Czy amantadyna leczy COVID-19? Są wyniki badań. Konferencja w Ministerstwie Zdrowia
- Wstępne wyniki badań nad amantadyną na próbie 149 chorych na COVID-19 przebywających w szpitalu pokazują, że nie ma różnic pomiędzy grupą osób leczonych amantadyną, a grupą pacjentów przyjmujących placebo - przekazał prof. Adam Barczyk. - To jednoznacznie przerywa dyskusje, pokazując czarno na białym, jakie są wyniki stosowania amantadyny w leczeniu szpitalnym - wskazał z kolei prezes Agencji Badań Medycznych Radosław Sierpiński.
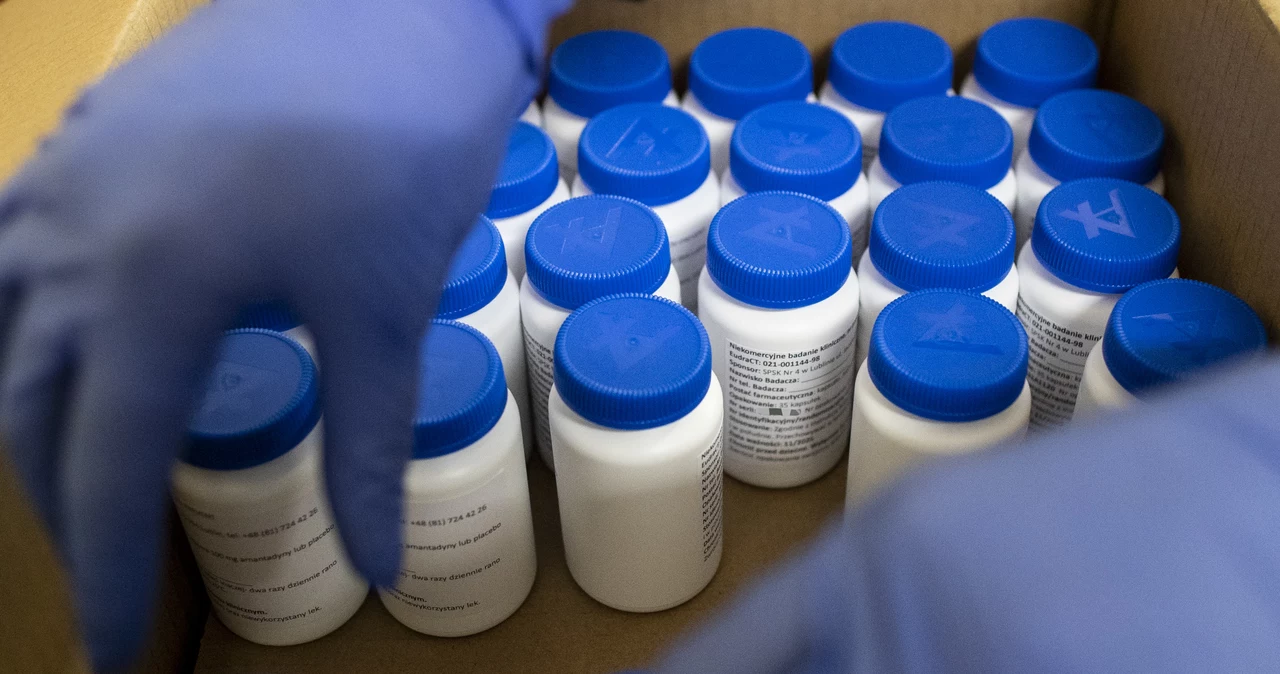
W konferencji prasowej na temat amantadyny w resorcie zdrowia wzięli udział wiceminister zdrowia Maciej Miłkowski, prof. Adam Barczyk ze Śląskiego Uniwersytetu Medycznego, prezes Agencji Badań Medycznych Radosław Sierpiński i rzecznik praw pacjenta Bartłomiej Chmielowiec.
Badania kliniczne amantadyny
Prof. Adam Barczyk, koordynator badania, podkreślił, że w działania było zaangażowanych kilkaset osób - w tym lekarzy i pielęgniarek, którym podziękował.
Zbadano 149 chorych, z czego 78 osób otrzymało amantadynę, a 71 placebo. - Badanie było prowadzone w populacji pacjentów ze szpitalnym covidem, czyli ci którzy są na początku choroby, ale pojawiały się już ciężkie bądź umiarkowane objawy - wyjaśniał prof. Adam Barczyk.
Leczenie amantadyną? Nie różni się od placebo
- Wstępne wyniki badań nad amantadyną pokazują, że nie ma różnic pomiędzy grupą osób leczonych amantadyną, a grupą pacjentów przyjmujących placebo - wskazał naukowiec. W związku z tym - jak przekazał prof. Barczyk - zwrócił się on do prezesa Agencji Badań Medycznych o zaprzestanie rekrutacji pacjentów i zakończenie badania.
Oglądaj transmisję:

- To badanie kliniczne jednoznacznie przerywa dyskusje, pokazując czarno na białym, jakie są wyniki stosowania amantadyny w leczeniu szpitalnym. (...) Cieszę się, że jako urząd spełniliśmy te rolę, jaką jest szukanie odpowiedzi na wątpliwości społeczne i ucięcie spekulacji - wskazał z kolei Radosław Sierpiński, prezes Agencji Badań Medycznych, która finansowała badania.
Amantadyna a COVID-10. Chmielowiec: Nie ma dowodów na skuteczność i bezpieczeństwo
Jak powiedział, drugą część badania prowadzono na pacjentach leczonych ambulatoryjnie, w przychodni. Na rezultaty tego badania jeszcze czekamy. - Pojawią się na dniach - zapowiedział Sierpiński.
Głos zabrał także Bartłomiej Chmielowiec, rzecznik praw pacjenta. Jak wskazał, nie ma na ten moment dowodów potwierdzających skuteczność i bezpieczeństwo stosowania amantadyny u chorych na COVID-19.
Amantadyna. Zakaz stosowania u pacjentów z COVID-19
- W związku z tym wydałem decyzję, w której uznałem, że placówka medyczna Optima z Przemyśla poprzez stosowanie u chorych na COVID-19 amantadyny narusza zbiorowe prawo pacjentów do leczenia zgodnie z aktualną wiedzą medyczną - powiedział Chmielowiec. Jednocześnie podkreślił, że zakaz stosowania amantadyny u pacjentów z COVID-19 może być zniesiony, jeśli pojawią się "rzetelne i wiarygodne dane naukowe" na temat skuteczności tego leku u pacjentów z covidem.
Na razie jednak, jak wskazał rzecznik, amantadyna nie jest zalecana w leczeniu COVID-19 w żadnej rekomendacji, również za granicą. - Poza nieskutecznością tej terapii może ona nieść zagrożenia dla życia i zdrowia pacjenta, dawać złudne poczucie skutecznego leczenia, powodując opóźnienie w podjęciu skutecznej terapii - dodał.
Także wiceminister Miłkowski przypomniał, że amantadyna w przebiegu COVID-19 nie jest i nie była zalecana.
Amantadyna. Cessak: Roma locuta, causa finita
Do sprawy odniósł się także na Twitterze prezes Urzędu Rejestracji Produktów Leczniczych (URPL) Grzegorz Cessak.
"Smutny dzień dla wszystkich entuzjastów stosowania amantadyny w leczeniu COVID-19. Roma locuta, causa finita" - napisał, załączając tweet z briefingu resortu.
Łacińską formułę "Roma locuta causa finita" tłumaczy się: "Rzym przemówił, sprawa zakończona". Oznaczała ona, że decyzja papieża jest ostateczna i niepodważalna.
Amantadyna a COVID-19. Badania kliniczne
Amantadyna to lek stosowany w neurologii, ale substancja ta wykorzystywana jest również przy leczeniu pacjentów z COVID-19.
Ministerstwo Zdrowia poinformowało w grudniu 2021 r., że badania amantadyny prowadziły w Polsce dwa podmioty - Samodzielny Publiczny Szpital Kliniczny nr 4 w Lublinie i Górnośląskie Centrum Medyczne im. prof. Leszka Gieca w Katowicach.
Zaznaczono wówczas, że przedstawienie wstępnych wyników będzie możliwe po osiągnięciu statystycznie istotnej liczby zrekrutowanych i przebadanych pacjentów.
Amantadyna. Ograniczenia w aptekach
Resort zdrowia 8 grudnia 2021 r. wprowadził ograniczenia dotyczące amantadyny poza wskazaniami medycznymi do jej stosowania.
W opublikowanym obwieszczeniu resort podał, że od 10 grudnia 2021 r. liczba wydawanego na jednego pacjenta w aptece ogólnodostępnej lub w punkcie aptecznym produktu leczniczego Viregyt-K (Amantadini hydrochloridum) zostanie ograniczona do nie więcej niż 3 opakowań po 50 kapsułek na 30 dni.
Zdecydowano też, że Viregyt-K, może być ordynowany i wydawany wyłącznie w następujących wskazaniach objętych refundacją: choroba i zespół Parkinsona oraz dyskineza późna u osób dorosłych - leczenie.